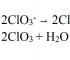Възможна е химична реакция между вещества с формулата, която
ЧАСТ А. Тестове с множествен избор
1. Зарядът на ядрото на атом +8 имат атомите на химичен елемент:
2. Броят на общите електронни двойки в хлорна молекула:
3. Ковалентна полярна връзка съществува в молекула на вещество, чиято формула е:
4. Степента на окисление на азота в редица вещества, чиито формули са N2-NO-NO2-HNO3:

5. Структурна формула на водородното съединение на елемент Е от основната подгрупа на група VI на Периодичната таблица:

6. Уравнението на химичната реакция H2S + C12 = 2HC1 + Sсъответства на схемата за преобразуване на хлор:

7. Вещество X в поредицата от трансформации CO2 → X → Ca (HCO3) 2 → CO2 има формулата:
8. Реактивът за хлоридния анион е катионът:
9. Възможна е химична реакция между вещества, чиито формули са:
10. Азотният оксид (IV) се образува при взаимодействието на вещества, чиито формули:
ЧАСТ Б. Задачи със свободен отговор
11. Запишете уравненията на реакциите, с които можете да извършите трансформациите по схемата:

12. Трансформирайте 2 от задача 11 от гледна точка на IDA.
Опция 1.
1. Зарядът на ядрото на атом +8 имат атомите на химичен елемент:
Б. Кислород.
2. Броят на общите електронни двойки в хлорна молекула:
В три часа.
3. Ковалентна полярна връзка съществува в молекула на вещество, чиято формула е:
Б. CO2.
4. Степента на окисление на азота в редица вещества, чиито формули са N2-NO-NO2-HNO3:
A. Увеличава се от 0 до +5.
5. Структурна формула на водородното съединение на елемент Е от основната подгрупа на група VI на Периодичната таблица:
V. N-E-N.
6. Уравнението на химичната реакция H2S + C12 = 2HC1 + S съответства на схемата за преобразуване на хлор:
A. Cl0 → Cl-1
7. Вещество X в поредицата от трансформации CO2 → X → Ca (HCO3) 2 → CO2 има формулата:
B. CaCO3.
8. Реактивът за хлоридния анион е катионът:
B. Ag +.
G. H2SO4 и MgO.
10. Азотният оксид (IV) се образува при взаимодействието на вещества, чиито формули:
B. HNO3 (конц.) и Ag.
2P + 3Zn = Zn3P2
Zn3P2 + 3H2O + 4O2 = 3Zn (OH) 2 + P2O5
P2O5 + 3H2O = 2H3PO4
2H3PO4 + 6Na = 2Na3PO4 + 3H2
Na3PO4 + 3AgNO3 = Ag3PO4 ↓ + 3NaNO3
Zn3P2-3 + 3H2O + 4O20 = 3Zn (OH) 2 + P2 + 5O5-2
O2 0 → 2O -2 +2 e, окислител
P -3 → P +5 - 8 e, редуциращ агент
Na3PO4 + 3AgNO3 = Ag3PO4 ↓ + 3NaNO3
3Na + + PO4 3- + 3Ag + + 3NO3- = Ag3PO4 ↓ + 3Na + + 3NO3-
PO4 3- + 3Ag + = Ag3PO4 ↓
14. Изчислете масата (в kg) на хлороводорода, която се получава при взаимодействието на 4,48 m3 хлор с излишък от водород.
n (Cl2) = 4480 dm3 / 22,4 dm3 / mol = 200 mol
n (НСl) = 2n (Cl2) = 400 mol
m (HCl) = 400 mol * 36,5 g / mol = 14600 g = 14,6 kg
15. Име химичен елемент, който има изотоп, в чието ядро няма неутрони.
водород
Вариант 2.
ЧАСТ А. Тестове с множествен избор
1. Зарядът на ядрото на атом +17 има атомите на химичен елемент:
G. Хлор.
2. Броят на обикновените електронни двойки в една водородна молекула:
А. 1.
3. Ковалентна неполярна връзка съществува в молекула на вещество, чиято формула е:
A. N2.
4. Степента на окисление на фосфора в редица вещества, чиито формули са Ca3P2-P-P2O3-P2O5:
Б. Увеличава се от -3 до +5.
5. Структурна формула на водородното съединение на елемент Е от основната подгрупа на група V на Периодичната система:
G. N-E-N.
Х
6. Уравнението на химичната реакция 2SО2 + О2 = 2SO3 съответства на схемата за преобразуване на сярата:
Б. S + 4 → S + 6.
7. Вещество X в поредицата от трансформации N2 → NH3 → X → NO2 има формулата:
Б. НЕ
8. Реактивът за карбонатния анион е катионът:
A. N +.
9. Възможна е химична реакция между вещества, чиито формули са:
B. P2O5 и NaOH.
10. Серният оксид (IV) не се образува от взаимодействието на вещества, чиито формули:
G. CaCO3 и H2SO4.
ЧАСТ Б. Задачи със свободен отговор
1. Mg + S = MgS
2,2 MgS + ЗО2 = 2MgО + 2SО2,
3,2SO2 + O2 = 2SO3
4.SO3 + Na2O = Na2SO4
5. Na2SO4 + BaCl2 = BaSO4 ↓ + 2NaCl
12. Трансформирайте 2 от задача 11 от гледна точка на IDA.
2 MgS-2 + 3020 = 2MgO-2 + 2S + 4O2-2,
S-2 → S + 4, -6e, редуциращ агент
O20 → 2O-2 + 2 * 2e, окислител
13. От задача 11 изберете реакцията на йонообмен и я запишете в йонна форма.
Na2SO4 + BaCl2 = BaSO4 ↓ + 2NaCl
SO42- + Ba2 + = BaSO4 ↓
14. Изчислете масата (в kg) на амоняка, която се получава при взаимодействието на 2 kmol азот с излишък от водород.
N2 + 3H2 = 2NH3
n (NH3) = 2n (N2) = 4kmol = 4000 mol
m (NH3) = 4000 mol * 17 g / mol = 68000 g = 68 kg.
15. Назовете химичен елемент, който никога не проявява положителна степен на окисление в съединенията.
Флуор
Вариант 3.
ЧАСТ А. Тестове с множествен избор
1. Зарядът на ядрото на атом +14 има атомите на химичен елемент:
Б. Силиций.
2. Броят на общите електронни двойки в бромната молекула:
А. 1.
3. В вещество съществува ковалентна полярна връзка, чиято формула е:
B. H2S.
4. Степента на окисление на сярата в редица вещества, чиито формули са SO3-SO2-S-H2S:
G. Намалява от +6 до -2.
5. Структурна формула на водородното съединение на елемент Е от основната подгрупа на група VII на Периодичната система:
A. N-E.
6. Уравнението на химичната реакция 4NH3 + 5О2 = 4NO + 6Н2О съответства на схемата за преобразуване на азота:
Б. N-3 → N + 2.
7. Вещество X в поредицата от трансформации PH3 → P2O5 → X → Ca3 (PO4) 2 има формулата:
A. H3PO4.
8. Реактивът за сулфатния анион е катионът:
B. Ba2 +.
9. Възможна е химична реакция между вещества, чиито формули са:
A. CO2 и NaOH.
10. Въглеродният окис (IV) се образува при взаимодействието на вещества, чиито формули:
B. CaCO3 и HC1.
ЧАСТ Б. Задачи със свободен отговор
11. Запишете уравненията на реакциите, с които можете да извършите трансформациите по схемата:
SiH4 → SiО2 → Na2SiО3 → H2SiО3 → SiО2 → Si.
1.SiH4 + 2O2 = SiO2 + 2H2O
2.SiO2 + Na2O = Na2SiO3
3. Na2SiO3 + 2HCl = H2SiO3 ↓ + 2NaCl
4.H2SiO3 = SiO2 + H2O
5.SiO2 + 2C ---> Si + 2CO
12. Трансформирайте 5 от задача 11 от гледна точка на IDA.
Si + 4O2 + 2C0 ---> Si0 + 2C + 2O
Si + 4 → Si0 + 4e, окислител
C0 → C + 2 -2e, редуциращ агент
13. От задача 11 изберете реакцията на йонообмен и я запишете в йонна форма.
Na2SiO3 + 2HCl = H2SiO3 ↓ + 2NaCl
SiO32- + 2H + = H2SiO3 ↓
14. Изчислете масата (в kg) на амониевия хлорид, който се образува при взаимодействието на 11,2 m3 хлороводород с излишък от амоняк.
HCl + NH3 = NH4Cl
n (HCl) = n (NH4Cl) = 11200 dm3 / 22,4 dm3 / mol = 500 mol
m (NH4Cl) = 500 mol * 56,5 g / mol = 28250 g = 28,250 kg.
15. Подредете химичните елементи фосфор, кислород, сяра, хлор в реда на нарастване на неметалните свойства.
Фосфор, сяра, кислород, хлор
Вариант 4.
ЧАСТ А. Тестове с множествен избор
1. Зарядът на ядрото на атом +16 има атомите на химичен елемент:
V. Sera.
2. Броят на общите електронни двойки в азотната молекула:
В 3.
3. В вещество съществува ковалентна неполярна връзка, чиято формула е:
B. O2.
4. Степента на окисление на въглерода в редица вещества, чиито формули са СН4-С-СО-СО2:
Б. Увеличава се от -4 до +4.
5. Структурната формула на водородното съединение на елемента Е от основната подгрупа от група IV на Периодичната система:
V. N-E-N
6. Уравнението на химичната реакция Cu + 4HNO3 = CU (NO3) 2 + 2NO2 + 2H2O съответства на схемата за преобразуване на азота:
G. N + 5 → N + 4.
7. Вещество X в поредицата от трансформации S → S02 → X → Na2SO3 има формулата:
G. H2SO3.
8. Реактивът за фосфатния анион е катионът:
G. Ag +.
9. Възможна е химична реакция между вещества, чиито формули са:
Б. CO2 и Ca (OH) 2.
10. Силициевата киселина се образува при взаимодействието на вещества, чиито формули:
B. Na2SiO3 и HC1.
ЧАСТ Б. Задачи със свободен отговор
11. Запишете уравненията на реакциите, с които можете да извършите трансформациите по схемата:
N2 → NH3 → NO → NO2 → HNO3 → KNO3.
1.N2 + 3H2 = 2NH3
2,4NH3 + 5O2 = 4NO + 6H2O
3.2NO + O2 = 2NO2
4.4NO2 + О2 + 2Н2О → 4HNO3
5.HNO3 + KOH = KNO3 + H2O
12. Трансформация 2 в задача 11 разгледайте от гледна точка на IDU.
4N-3H3 + 5O20 = 4N + 2O-2 + 6H2O
N-3 -> N + 2, -5e, редуциращ агент
O20-> 2O-2, + 2 * 2e, окислител
13. От задача 11 изберете реакцията на йонообмен и я запишете в йонна форма.
HNO3 + KOH = KNO3 + H2O
H + + OH- = H2O
14. Изчислете масата (в kg) на серен (IV) оксид, образуван при изгарянето на 4,48 m3 сероводород в излишък от кислород.
2H2S + 3O2 = 2SO2 + 2H2O
n (H2S) = n (SO2) = 44800 dm3 / 22,4 dm3 / mol = 2000 mol
m (SO2) = 2000 mol * 64 g / mol = 128000 g = 128 kg
15. Назовете най-често срещания химичен елемент:
А. В земната кора:
кислород
Б. Във Вселената:
водород
2. NaCl (p-p) и H2SO4 (p-p)
3. BaCl₂ (p-p) и Cu (NO₃) ₂ (p-p)
4.KNO3 (p-p) и KOH
5. Na2SO3 и Ca (NO3)₂
Схемата за преобразуване на сяра S ⁺⁶ -> S ⁺⁴ (неразбираеми квадрати поради проблеми с кодирането, очевидно - това са знаците плюс, които се показват по този начин):
1.S + O2 = SO2
2.Cu + 2H₂SO₂ (конц.)
3.2SO2 + O2 = 2SO3
4.H2SO4 + BaCl₂ = BaSO4 + 2HCl
5.C + 2H₂SO₄ (край) = CO₂ + 2SO₂ + 2H₂O
Азотът е редуциращ агент в реакциите, чиито уравнения са:
1,4NO2 + O2 + 2H2O = 4HNO3
2.4NH3 + 5O2 = 4NO + 6H2O
3,2Cu (NO₃) ₂ = 2CuO + 4NO₂ + O₂
4. NH4Cl = NH3 + HCl
5.4HNO3 = 4NO2 + 2H2O + O2
Редокс реакциите включват реакции, чиито уравнения са:
1. BaCl₂ + 2AgNO₂ = 2AgCI + Ba (NO₃) ₂
2. CaCO₃ = CaO + CO₂
3. CuO + H2 = Cu + H2O
4,4HNO3 = 4NO₂ + 2H2O + O₂
5. Na2O + H2SO4 = Na2SO4 + H2O
Натриевият оксид (NA₂O) не взаимодейства с:
1. AlCl₃ - алуминиев хлорид
2.N₂O₅ - азотен оксид
3. MgO - магнезиев оксид
4. HCl - солна киселина
5. H2O - вода
Азотният оксид 5 (N₂O₅) реагира с вещества, чиито формули са:
1. NH3
2.H2O
3. Ba (OH) ₂ (p-p)
4. O₂
5. HCI (p-p)
Всяко от веществата, чиито формули са H₂O, CaO, KOH, ще взаимодейства:
1. Въглероден оксид (4)
2. Въглероден оксид (2)
3. Азотен оксид (4)
4. Меден оксид (2)
5. Азотен оксид (2)
Реакции между вещества, чиито формули:
1. NaOH и HNO3
2. HC₃ и CaCO3
3. CaSO₄ и BaCl₂
4. KNO3 и KOH
5. Na2SO3 и Ca (NO3)₂
1 (2 точки). Атомите на химичен елемент имат заряд на ядрото на атома +17:
А. Азот. Б. Кислород. V. Sera. G. Хлор.
2 (2 точки). Броят на общите електронни двойки в молекулата на водорода:
A.1. B.2. В 3. Г.4.
3 (2 точки). Ковалентна неполярна връзка съществува в молекула на вещество, чиято формула е:
A. N2 B. CH4 C. HCI. G. Na2S.
4 (2 точки). Степента на окисление на фосфора в редица вещества, чиито формули
Ca3P2 - P - P2O3 - P2O5
A. Увеличава се от 0 до +5. Б. Увеличава се от -3 до +5.
B. Намалява от +6 до -2. G. Увеличава се от -4 до +4.
5 (2 точки). Структурна формула на водородното съединение на елемента Е от основната подгрупа
Група V на периодичната таблица:
A. N-E H V. N-E-N
B. N-E-N G. N-E-N
6 (2 точки). Уравнение на химичната реакция 2SO2 + O2 = 2SO3
съответства на схемата за преобразуване на сярата:
A. S0-S + 4 B. S-2-S + 4 B S + 4-S + 6 D. S + 6-S + 4
7 (2 точки). Вещество X в поредицата от трансформации N2 → NH3 → X → NO2
има формулата:
A. NO2 B. NO B. N2O3 D. N2O5
8 (2 точки). Реактивът за карбонатния анион е катионът:
A. H + B. NH + 4. B. K + G. Na +
9 (2 точки). Възможна е химична реакция между вещества, чиито формули са:
И SiO2 и H2O. B. P2O5 и NaOH.
Б. CO2 и SO2. G. H2SiO3 и Mg.
10 (2 точки). Серният оксид (IV) не се образува от взаимодействието на вещества, чиито формули:
A.S и O.B. Cu и H2SO4 (CONC). B. Hg и H2SO4 (CONC). G. CaCO3 и H2SO4.
ЧАСТ Б. Задачи със свободен отговор
11 (6 точки). Запишете уравненията на реакцията, с които можете да извършите трансформациите по схемата:
S → MgS → SO2 → SO3 → Na2SO4 → BaSO4
12 (12 точки). Разгледайте трансформацията 2 от задача 11 от гледна точка на OVR.
13 (6 точки). От задача 11 изберете йонообменната реакция и я запишете в йонна форма.